TRAS UN LARGO Y POLÉMICO PROCESO
EEUU venderá la 'Viagra' femenina para mujeres con bajo deseo sexual
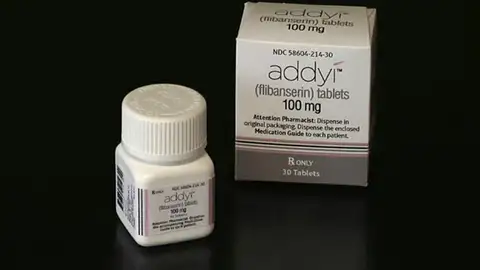
Es una pequeña píldora de color rosa pensada para mujeres premenopáusicas que sufran una pérdida repentina de cualquier deseo de practicar sexo, aunque muchas quieren ver en este medicamento como un estimulante de la líbido femenina. Los médicos advierten de los efectos secundarios, aunque ya ha logrado revolucionar el sector farmacéutico en EEUU. Su llegada a España aún tendrá que esperar.
Publicidad
La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) dio luz verde a mediados de agosto a la comercialización de la flibanserina, un nombre detrás del que se esconde la primera píldora en el mercado que incrementa el deseo sexual de la mujer, y dos meses más tarde ha llegado a las farmacias de ese país. Son pequeñas píldoras de color rosa pensadas para ser administradas diariamente a mujeres premenopáusicas que sufran un desorden de anorexia sexual, es decir la pérdida repentina de cualquier deseo de practicar sexo.
Esta 'viagra' femenina modifica tres sustancias químicas claves para el cerebro: la dopamina y la norepinefrina, las cuales aumenta, y la serotonina, la cual disminuye. Lo que consigue es incrementar la libido en las mujeres y su deseo sexual. Su coste es 400 dólares al mes, aunque para quienes tengan cobertura médica puede llegar a recudirse hasta los 30 dólares.
Hasta llegar a su venta pública desde el pasado 17 de octubre, Addyi, que es su nombre comercial, ha tenido que superar un largo y polémico proceso hasta que un grupo de expertos recomendara su aprobación en junio. La Organización Nacional para la Mujer y otras asociaciones feministas acusaron a la FDA de estar sometiendo a mayores observaciones esta medicación que las diseñadas para incrementar la libido masculina, como Viagra y Cialis.
Los principales responsables del retraso en su aprobación han sido los efectos secundarios, que en este caso son posibles desmayos y disminución de la presión arterial, riesgos que aumentan con el consumo de alcohol y con el uso de otros medicamentos que interfieren con la descomposición de Addyi en el organismo. La FDA rechazó en otras dos ocasiones anteriores el compuesto después de que otros grupos de asesoramiento concluyeran que había dudas sobre su seguridad, y no consideraba que hubiera pruebas suficientes que demostraran que el fármaco es eficaz para las mujeres con poco deseo sexual.
La doctora Janet Woodcock, directora del Centro de Evaluación e Investigación de Medicamentos (CDER) de la FDA, explicó que el tratamiento con Addyi sólo está "disponible a través de profesionales sanitarios certificados y farmacias certificadas". "Los pacientes y los médicos prescriptores deben comprender totalmente los riesgos asociados con el uso de Addyi antes de considerar el tratamiento", advirtió Woodcock.
Publicidad