Coronavirus
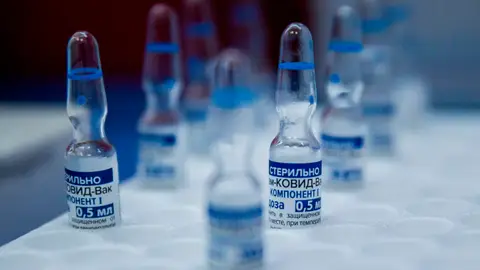
La EMA inicia una "revisión continua" de la vacuna rusa contra el coronavirus, Sputnik-V
Este proceso de "revisión continua" consiste en un análisis en tiempo real para comprobar la eficacia de la vacuna contra el coronavirus rusa y verificar que "los beneficios superan los riesgos" de ser así podría concluir con la autorización de la comercialización de la Sputnik-V en Europa.
Publicidad
La vacuna rusa contra el coronavirus podría estar un poco más cerca de comercializarse en Europa después de que la Agencia Europea del Medicamento haya iniciado un proceso de "revisión continua", un análisis en tiempo real, de los datos sobre la seguridad, la eficacia y la calidad de Sputnik-V.
La Agencia asegura que se ha dado el paso apoyándose "en los resultados de los estudios de laboratorio y los estudios clínicos en adultos" que el desarrollador del fármaco ha compartido con los científicos europeos de la EMA, información que ya está siendo analizada por sus expertos en su sede de Ámsterdam.
La EMA analizará si la vacuna contra el coronavirus Sputnik V "desencadena la producción de anticuerpos y células inmunes que se dirigen al SARS-CoV-2" y protege a las personas inoculadas, algo que la EMA evaluará primero "con los estándares habituales de la UE en cuanto a eficacia, seguridad y calidad".
La EMA no ha avanzado un plazo determinado para concluir dicho análisis y continuará hasta que haya suficiente información disponible para presentar una solicitud formal de autorización de comercialización en la UE. La agencia evaluará los datos a medida que vayan estando disponibles, hasta poder decidir "si los beneficios superan los riesgos" de este fármaco, lo que también permitirá en el futuro a los desarrolladores presentar una solicitud para que la EMA estudie la posibilidad de dar luz verde a la Comisión Europea para que emita una licencia de uso condicional en la UE.
Actualmente se encuentran en proceso de evaluación las vacunas contra la COVID-19 desarrolladas por CureVac y Novavax, también aunque en una fase más avanzada el suero de Janssen que ya presentó formalmente una solicitud para que la EMA estudie dar luz verde a la Comisión para que esta autorice una licencia de uso condicional del fármaco el próximo 11 de marzo. De lograrlo se convertiría en la cuarta vacuna disponible en Europa junto a Pfizer/BioNtech, Moderna y AstraZeneca.
Más Noticias
-
 Última hora del brote de hantavirus en directo: Clavijo confirma tras la reunión con Sanidad que el crucero no atracará en Tenerife, "solo fondeará"
Última hora del brote de hantavirus en directo: Clavijo confirma tras la reunión con Sanidad que el crucero no atracará en Tenerife, "solo fondeará"
-
 El video del capitán del crucero con hantavirus alertando del primer muerto: "No es infeccioso. El barco está seguro"
El video del capitán del crucero con hantavirus alertando del primer muerto: "No es infeccioso. El barco está seguro"
-
 Más mortal, sin vacuna ni tratamiento: parecidos y diferencias entre el hantavirus y el COVID-19
Más mortal, sin vacuna ni tratamiento: parecidos y diferencias entre el hantavirus y el COVID-19
Recuerda que puedes consultar toda la información sobre el calendario y proceso de vacunación contra el coronavirus en España y el resto del mundo en nuestra herramienta de 'CuentaVacunas'.
Publicidad